Accueil > 01 - Livre Un : PHILOSOPHIE > L’image du chaos déterministe > Qu’est-ce que le mouvement brownien ?
Qu’est-ce que le mouvement brownien ?
vendredi 26 mars 2010, par
Les corpuscules de Brown au microscope

À l’été 1827, le naturaliste écossais Robert Brown aperçut dans le fluide situé à l’intérieur des grains de pollen de la Clarkia pulchella, de très petites particules agitées de mouvements apparemment chaotiques.
Mouvement de sphères (20 nm de diamètre) de latex fluorescentes dans de l’eau.

D’où vient l’énergie de ce mouvement désordonné et permanent de très petits grains ? De l’agitation des molécules. Mais comment peut-elle elle-même être aussi désordonnée et permanente ? Du fait de l’énergie du vide quantique !
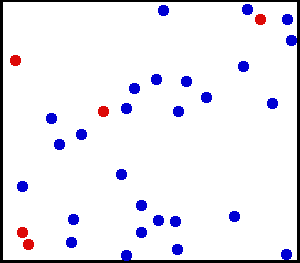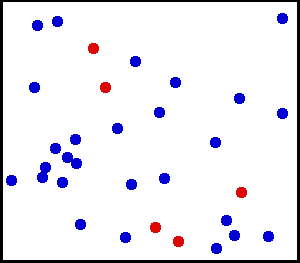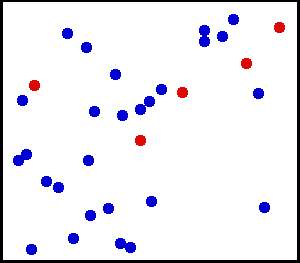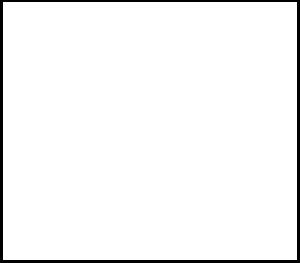
Le mouvement agité des corpuscules de Brown, en jaune puis en bleu, et l’agitation des molécules qui cause le mouvement brownien


Mouvement brownien et molécules, par Jean Perrin, 1923 sur la Vidéothèque du CNRS
Mouvement brownien et probabilités, le film
« Le monde des atomes et l’agitation moléculaire », Jean Perrin
« Mouvement brownien et réalité moléculaire », Jean Perrin
« Le monde des atomes et l’agitation moléculaire », Jean Perrin
« Mouvement brownien et grandeurs moléculaires », Jean Perrin
Films d’archives sur les travaux de Jean Perrin
Jean Perrin – Extraits de « Les atomes » :
« Mouvement brownien – émulsions
« Historique et caractères généraux
« Le mouvement brownien –
« L’agitation moléculaire échappe à notre perception directe comme le mouvement des vagues de la mer à un observateur trop éloigné. Cependant si quelque bateau se trouve alors en vue, le même observateur pourra voir un balancement qui lui révèlera l’agitation qu’il ne soupçonnait pas. Ne peut-on de même espérer, si des particules microscopiques se trouvent dans un fluide, que ces particules, encore assez grosses pour être suivies sous le microscope, soient déjà assez petites pour être notablement agitées par les chocs moléculaires ?
Cette question aurait pu conduire à la découverte d’un fait merveilleux, que nous a révél l’observation microscopique, et qui nous donne une vue profonde sur les propriétés de l’état fluide.
A l’échelle ordinaire de nos observations, toutes les parties d’un liquide en équilibre nous semblent immobiles. Si l’on place dans ce liquide un objet quelconque plus dense, cet objet tombe, verticalement s’il est sphérique, et nous savons bien qu’une fois arrivé au fond du vase, il y reste, et ne s’avise pas de remonter tout seul.
Ce sont là des notions bien familières, et pourtant elles ne sont bonnes que pour les dimensions auxquelles nos organes sont accoutumés. Il suffit en effet d’examiner au microscope de petites partiucles placées dans l’eau pour voir que chacune d’elles, au lieu de tomber régulièrement, est animée d’un mouvement très vif et parfaitement désordonné. Elle va et vient en tournoyant, monte, descend, remonte encore, sans tendre aucunement vers le repos. C’est le « mouvement brownien », ainsi nommé en souvenir du botaniste anglais Brown, qui le découvrit en 1827, aussitôt après la mise en usage des premiers objectifs achromatiques.
Cette découverte si remarquable attira peu l’attention. Les physiciens qui entendaient parler de cette agitation la comparaient, je pense, au mouvement des poussières qu’on voit à l’œil nu se déplacer dans un rayon de soleil, sous l’action des courants d’air qui résultent de petites inégalités dans la pression ou la température. Mais, en ce cas, des particules voisines se meuvent à peu près dans le même sens et dessinent grossièrement la forme de ces courants d’air. Or il est ompossible d’observer quelque temps le mouvement brownien sans s’apercevoir qu’au contraire il y a indépendance complète des mouvements de deux particules, même quand elles s’approchent à une distance inférieure à leur diamètre (Brown, Wiener, Gouy).
L’agitation ne peut donc être due à des trépidations de la plaque qui porte la gouttelette observée, car ces trépidations, quand on en produit exprès, produisent précisément des courants d’ensemble, que l’on reconnaît sans hésitation et que l’on voit simplement se superposer à l’agitation irrégulière des grains. D’ailleurs, le mouvement brownien se produit sur un bâti bien fixe, la nuit, à la campagne, aussi nettement que le jour, à la ville, sur une table sans cesse ébranlée par le passage de lourds véhicules (Gouy). De même, il ne sert à rien de se donner beaucoup de peine pour s’assurer l’uniformité de température de la gouttelette : tout ce qu’on gagne est encore seulement de supprimer des courants de convection d’ensemble parfaitement reconnaissables, et sans aucun rapport avec l’agitation irrégulière observée (Wiener, Gouy). On ne gagne rien non plus en diminuant extrêment l’intensité de la lumière éclairante, ou en changeant sa couleur (Gouy).
Bien entendu, le phénomène n’est pas particulier à l’eau, mais se retrouve dans tous les fluides, d’autant plus actif que ces fluides sont moins visqueux. Aussi est-il à peine perceptible dans la glycérine, et au contraire extrêment vif dans les gaz (Bodoszewski, Zsigmondy).
Incidemment, j’ai pu observer pour des sphérules d’eau supportés par les « tâches noires » des bulles de savon. Ces sphérules étaient de 100 à 1 000 fois plus épais que la lame mince qui leur servait de support. Ils sont donc à peu près aux tâches noires ce qu’une orange est à une feuille de papier. Leur mouvement brownien, négligeable dans la direction perpendiculaire à la pellicule (à peu près comme il le serait dans un gaz).
Dans un fluide donné, la grosseur des grains importe beaucoup, et l’agitation est d’autant plus vive que les grains sont plus petits. Cette propriété fut signalée par Brown, dès le premier instant de sa découverte. Quant à la nature des grains, elle paraît avoir peu d’influence, si elle en a. Dans un même fluide, deux grains s’agitent de même quand ils ont la même taille, quelle que soit leur substance et quelle que soit leur densité (Jevons, Ramsay, Gouy). Et, incidemment, cette absence d’influence de la nature des grains élimine toute analogie avec les déplacements de grande amplitude que subit un morceau de camphre jeté sur l’eau, déplacements qui dureste finissent par s’arrêter (quand l’eau est saturée en camphre).
Enfin, précisément, - et ceci est peut-être le caractère le plus étrange et le plus véritablement nouveau – le mouvement brownien ne s’arrête jamais. A l’intérieur d’une cellule close (de manière à éviter l’évaporation), on peut l’observer pendant des jours, des mois, des années. Il se manifeste dans des inclusions liquides enfermées dans le quatz depuis des milliers d’années. Il est « éternel et spontané ».
Tous ces caractères forcent à conclure avec Wiener (1863) que « l’agitation n’a pas son origine dans les particules, ni dans une cause extérieure au liquide, mais doit être attribuée à des mouvements internes, caractéristiques de l’état fluide », mouvement que les grains suivent d’autant plus fidèlement qu’ils sont plus petits.
Nous atteignons là une propriété essentielle de ce qu’on appelle un fluide en équilibre : ce repos apparent n’est qu’une illusion due à l’imperfection de nos sens, et correspond, en réalité, à un certain régime permanent de violente agitation désordonnée. »
Perrin, "Les atomes"
Le mouvement brownien est la découverte qu’au sein de la stabilité, on trouve l’instabilité permanente, que l’ordre a pour origine le désordre et que l’irréversibilité est fondée sur la réversibilité, etc... En somme, il est l’illustration de la dialectique fondamentale de la matière... Et, au-delà de la matière pesante et durable, il s’agit de la dialectique du vide quantique car c’est lui qui, étant sans cesse agité, agite les molécules en permanence, sans quoi leurs chocs auraient fini par les amener à un état stable...
Si, une fois atteint un état stable, l’agitation venait seulement de l’extérieur, la matière devrait atteindre un état complètement et durablement stable. Au lieu de cela, on constate une agitation permanente appelée mouvement brownien.
« L’état d’un liquide en repos et où règnerait une température uniforme devrait être absolument incompatible avec un changement quelconque ; car là où on ne saurait trouver de différences d’intensité, il ne peut y avoir non plus aucune cause de changement. Mais on peut rendre visible ce qui se passe à l’intérieur d’un liquide tel que l’eau, par exemple, en y suspendant des particules très nombreuses et très petites ou des gouttelettes d’un autre liquide tel que du mastic ou de la gomme goutte. Or le spectacle qui attend celui qui regarde une préparation de ce genre sous le microscope est de ceux qui ne peuvent s’oublier. Il semble que l’on pénètre dans un monde entièrement nouveau. Au lieu de l’immobilité sépulcrale qu’il était naturel d’imaginer, l’observateur assiste à la plus échevelée des sarabandes de la part des particules suspendues et, chose remarquable, les particules qui se démènent le plus follement sont justement les plus petites. Il est impossible de déceler de la part du liquide aucun frottement qui freinerait le mouvement. Si, par hasard, une particule vient à s’arrêter, une autre particule entre aussitôt à sa place dans la danse. Devant un tel spectacle, il est impossible de ne pas songer à l’activité fiévreuse d’une fourmilière que l’on aurait bouleversée avec un bâton. Mais tandis que les insectes finissent par se remettre peu à peu de leur excitation et même par perdre toute activité quand la nuit tombe, les particules ne montrent pas la moindre trace de fatigue tant que la température du liquide reste constante. Nous sommes donc en présence du « perpetuum mobile » au sens le plus strict du mot et non pas dans une des nombreuses acceptations figurées qui ont été données à ce terme.
L’explication de ce phénomène, découvert par le botaniste anglais Brown, a été donnée il y a déjà vingt-cinq ans par le français Gouy. D’après ce physicien, le mouvement brownien est causé par l’agitation thermique des molécules du liquide. Ces molécules invisibles, par leurs chocs incessants contre les particules visibles qui flottent disséminées parmi elles, provoquent les mouvements irréguliers observés. Mais la preuve décisive de l’exactitude de cette opinion n’a été apportée que tout récemment.
Einstein et Scholumowski sont en effet parvenus à formuler une théorie statistique du mouvement brownien dont on peut déduire les lois régissant la densité de répartition des particules, leurs vitesses, la valeur de leurs parcours et même la valeur de leurs rotations. Ces lois ont été brillamment vérifiées par l’expérience, grâce surtout aux travaux de Jean Perrin. »
Max Planck dans « Initiations à la physique »
MOUVEMENT BROWNIEN
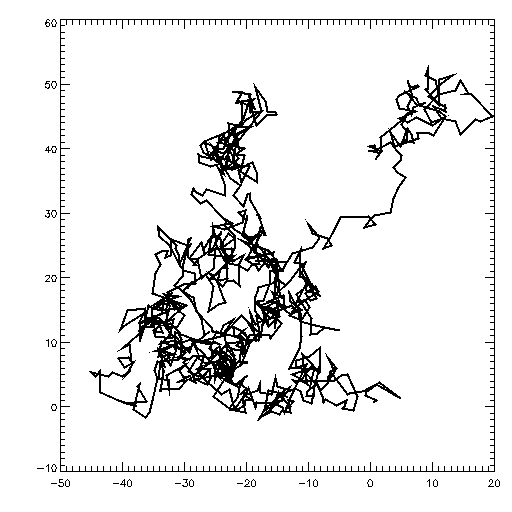
Le mouvement brownien correspond à l’agitation permanente des molécules de matière qui est non seulement brisé et aléatoire mais fractal, comme le montre le schéma en dessous :
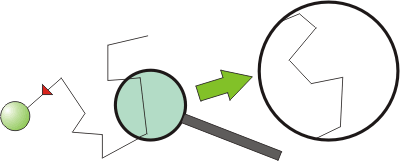
Jean Perrin en 1912 a relevé les trajets de certaines de ces particules et s’est rendu compte de la nature "fractale" de telles trajectoires. Les portions de trajectoires rectilignes observées toutes les 30 s deviennent elles-mêmes chaotiques lors d’un échantillonnage plus fin réalisé toutes les secondes par exemple.
Wendelin Werner et le caractère fractal du mouvement brownien
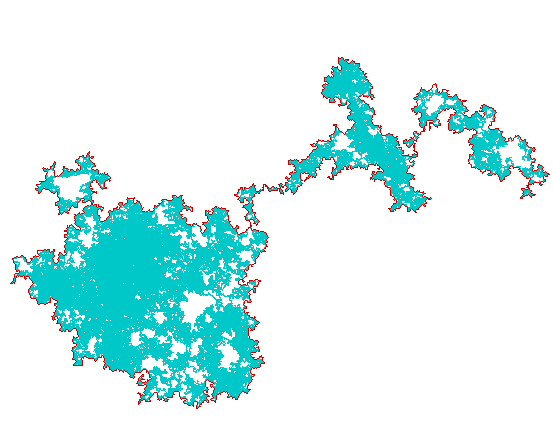
"Le mouvement des particules dans un liquide fut rendu manifeste, pour la première fois, par le mouvement brownien, phénomène remarquable, qui serait resté mystérieux et incompréhensible sans la théorie cinétique de la matière. Il a été observé par le botaniste Brown et expliqué 80 ans plus tard, au début de ce siècle. Le seul appareil nécessaire pour observer le mouvement brownien est le microscope, qui n’a même pas besoin d’être particulièrement puissant.
Brown a opéré avec des grains de pollen de certaines plantes, c’est-à-dire "des particules ou des granules d’une grosseur inaccoutumée, dont la longueur variait d’un quatre millième à un cinq millième d’un pouce."
Il dit en outre : "Pendant que j’examinais la forme de ces particules immergées dans l’eau, j’ai observé que beaucoup d’entre elles étaient manifestement en mouvement... Ces mouvements étaient tels que, après des observations souvent répétées, je fus persuadé qu’ils ne pouvaient provenir ni du courant du fluide, ni de son évaporation graduelle, mais qu’ils appartenaient à la particule même."
Ce que Brown observait, c’était l’agitation incessante de granules en suspension dans l’eau et visibles au microscope. C’est un spectacle impressionnant.
(...) Comment faut-il expliquer ce mouvement. Il paraît contradictoire à toute l’expérience antérieure. L’observation de la position d’une de ces particules en suspension pendant trente secondes par exemple révèle la forme fantastique de son chemin. La chose bouleversante, c’est le caractère de son mouvement apparemment éternel. Un pendule oscillant immergé dans l’eau s’arrête bientôt, si on ne lui imprime pas un mouvement par une force extérieure. l’existence d’un mouvement qui ne s’arrête jamais paraît contraire à toute l’expérience. Cette difficulté fut éclaircit par la théorie cinétique de la matière.
Quand on observe l’eau avec nos plus puissants microscopes, on ne voit pas de molécules en mouvement, telles que les dépeint la théorie cinétique de la matière. Il faut en conclure que si la théorie qui considère l’eau comme un amas de particules est juste, leur volume doit être au-delà des limites de visibilité des meilleurs microscopes. Restons néanmoins fidèles à la théorie et admettons qu’elle représente une image conforme à la réalité. Les particules browniennes visibles au microscope sont bombardées par les particules plus petites qui constituent l’eau. Le mouvement brownien existe, si les particules bombardées sont suffisamment petites. Il existe, parce que ce bombardement n’a pas lieu d’une manière uniforme de tous les côtés, et l’on ne peut pas, à cause de son caractère irrégulier et contingent, en établir une moyenne. Le mouvement observé est ainsi le résultat d’un mouvement non observable. Le comportement des grosses particules reflète jusqu’à un certain point celui des molécules et en constitue, pour ainsi dire, un grossissement si élevé qu’il devient visible au microscope. Le caractère irrégulier et contingent du chemin que parcourent les particules browniennes reflète une irrégularité similaire des chemins que parcourent les particules plus petites qui constituent la matière."
Albert Einstein et Leopold Infeld dans "L’évolution des idées en physique".
Le mouvement brownien, par Nicolas Vicente
Le mouvement brownien et l’apport d’Einstein
Le mouvement brownien vu par le mathématicien Jean-Pierre Kahane
MOTS CLEFS :
dialectique –
discontinuité –
physique quantique – relativité –
chaos déterministe – atome –
système dynamique – structures dissipatives – percolation –
non-linéarité – quanta –
émergence –
inhibition –
boucle de rétroaction – rupture de symétrie - turbulence – mouvement brownien –
le temps -
contradictions –
crise –
transition de phase – criticalité - attracteur étrange – résonance –
auto-organisation – vide - révolution permanente - Zénon d’Elée - Antiquité -
Blanqui -
Lénine -
Trotsky – Rosa Luxemburg –
Prigogine -
Barta -
Gould - marxisme - Marx - la révolution - l’anarchisme - le stalinisme - Socrate
« Pour illustrer ce qu’est un mouvement brownien, considérons le mouvement à ,la fois le plus simple et le plus aléatoire que l’on puisse concevoir et que l’on a pu observer. C’est celui où un objet représenté par un point fait, à chaque instant, un saut dans une direction quelconque dictée par le hasard et à une distance également soumise à une loi probabiliste qui élimine cependant toute chance de sauts de grande longueur.
Nous nous bornons tout d’abord à considérer des sauts de longueur constante ou à peu près constante. (…) Imaginons maintenant qu’un observateur reconstitue la trajectoire à partir de photos prises d’assez loin, tous les 100 pas, et comparons cette trajectoire avec celle que l’on obtiendrait en prenant des photos tous les 10.000 pas. Puisque l’observateur est assez loin, il ne pourra pas percevoir si la marche du piéton est le résultat d’une marche continue ou discontinue. On a ainsi représenté le mouvement brownien continu par une marche aléatoire discontinue à très petite échelle. Si maintenant on compare les photographies prises tous les 10, 100, 1000 ou 10.000 pas, on constate que ces trajectoires se ressemblent. On peut démontrer qu’elles sont en moyenne les mêmes à une dilatation près, c’est-à-dire à un changement d’échelle près. »
Bernard Sapoval dans « Universalités et fractales »
Des articles de Jean Perrin :
Mouvement brownien et grandeurs moléculaires
Mouvement brownien et réalité moléculaire

Messages
1. Qu’est-ce que le mouvement brownien ?, 22 mars 2009, 10:47
Qu’est-ce que le mouvement brownien ?
dans quels d’utres exemples peut-on trouver ce phénomène ?
n’est -il pas possible de comparer ce système à l’effet magnétique ? s de bko
1. Qu’est-ce que le mouvement brownien ?, 22 mars 2009, 13:43
Pour regarder le mouvement brownien
2. Qu’est-ce que le mouvement brownien ?, 12 mai 2009, 21:44, par Robert Paris
Le mouvement brownien a une apparence désordonnée. cependant il obéit à des lois. il permet de construire un certain type d’ordre. il sert ainsi d’image à différents types d’ordres issus du désordre. Le ferromagnétisme est effectivement un ordre issu du désordre.
2. Qu’est-ce que le mouvement brownien ?, 26 mars 2010, 10:38, par Robert Paris
A lire en complément :
ce texte
bonne lecture
3. Qu’est-ce que le mouvement brownien ?, 26 mars 2010, 10:39, par Toto
D’autres infos sur le mouvement brownien :
sur ce site
4. Qu’est-ce que le mouvement brownien ?, 26 mars 2010, 10:50, par Toto
Pourquoi parler de dialectique à propos du mouvement brownien ?
1. Qu’est-ce que le mouvement brownien ?, 26 mars 2010, 10:56, par Robert Paris
Ce qui caractérise la conception dialectique, c’est de faire appel à des contradictions internes.
Tout le monde admet que le mouvement peut venir de l’extérieur, par exemple quand un objet en heurte un autre mais seule la conception dialectique repose sur des contradictions internes de tous les systèmes.
Or, dans le cas du mouvement brownien comme dans nombre de phénomènes physiques, on constate des contradictions internes.
C’est également le cas en physique quantique puisque c’est à la fois onde et particule, à la fois étendu et localisé, etc...
Dans le mouvement brownien, la stabilité globale (température constante et uniforme) non seulement coexiste avec l’agitation mais est fondée dessus.
L’ordre et le désordre sont parfaitement imbriqués... La variation et la constance, le réversible et l’irréversible s’imbriquent également comme l’a parfaitement remarqué Max Planck.
2. Qu’est-ce que le mouvement brownien ?, 26 mars 2010, 12:38, par Robert Paris
Voici par exemple un commentaire sur le mouvement brownien à propos de son mélange de hasard et de nécessité, d’ordre et de désordre :
"Puisque l’effet du mouvement brownien est de classer statistiquement le fluide de telle sorte que la vitesse (ou la température ce qui revient au même) de l’ensemble de ses molécules soit toujours rangée en ordre bien progressif, il permet que les molécules se suivent toujours en bon ordre de vitesse. Mais puisque ce classement statistique n’est obtenu que par le mélange hasardeux perpétuel, le dérangement perpétuel du classement des molécules entre elles qui ne cessent de se brasser, il implique donc aussi que les molécules ne se suivent jamais en bon ordre de vitesse. Dans cette situation donc, toujours ça se suit sans se suivre."
5. Qu’est-ce que le mouvement brownien ?, 26 mars 2010, 12:46, par Toto
Quel rapport avec irréversibilité et réversibilité ?
1. Qu’est-ce que le mouvement brownien ?, 26 mars 2010, 12:48, par Robert Paris
Le mouvement brownien est apparemment réversible puisque le mouvement inverse de chaque particule est parfaitement possible. Mais l’évolution de l’ensemble du système est irréversible...
En 1872 Ludwig Boltzmann inventa le "théorème H" que l’on peut résumer comme suit : "Dans un mélange gazeux, l’entropie ne peut varier que dans un seul sens. Le mouvement des particules tend vers l’équilibre". En soumettant ce modèle aux scientifiques, Boltzmann allait s’opposer aux arguments de plusieurs physiciens, dont Zermelo et Poincaré. Le "théorème H" ou théorème de l’irréversibilité appliquait les lois de la physique classique. En fait il confortait les thèses mécanistes et réversibles de la physique. Boltzmann exprimait les lois de la thermodynamique en termes de mouvements de milliards de molécules régis par des lois statistiques (mécanique statistique). Mais avec des milliards de molécules, un gaz peut difficilement rester ordonner. Or depuis Galilée et Leibniz l’évolution dynamique des systèmes était réversible. Leibniz avait même énoncé le principe de "raison suffisante" car il était persuadé que la réversibilité déterministe allait de soi. Mais l’interprétation statistique de Boltzmann n’était pas valable pour les systèmes ouverts car ils n’avaient aucune tendance vers le désordre total.
En réponse à ces interprétations déterministes Poincaré énonça en 1890 le "théorème de récurrence”. Guidés par la tradition dynamique, Poincaré et Zermelo[2] supposaient qu’à tout moment l’état thermodynamique d’un système isolé pouvait se retourner et retrouver indéfiniment de fois un état très proche de sa valeur initiale. Ils considéraient de même que tous les états devaient se reproduire pourvu que l’on attende suffisamment longtemps. Ce “temps de Poincaré” mettait le doigt sur l’un des paradoxes de la thermodynamique. Mais les lois de la Nature nous permettent-elles de retourner la flèche du temps comme le théorème de Loschmidt le sous -entend ? Nous aimerions bien que le monde - et les lois de Joule et de Clausius en particulier - soient symétriques mais la réalité ne l’est pas.
C’est Léon Brillouin qui s’affranchit de ces difficultés en considérant qu’il existait des limites objectives à toute connaissance, limites fixées par le quantum d’action. La théorie classique devenait une approximation de la physique quantique. Au départ d’un processus thermodynamique ou quantique, il est vrai en théorie que chaque possibilité a une chance de s’actualiser. En pratique il y a réduction du paquet d’ondes, effondrement du nuage probabiliste dans une seule réalité. Ainsi, même si par nature les lois sont réversibles, les processus ne le sont pas, en particulier les structures dissipatives ou les phénomènes quantiques. Pour s’en convaincre, statistiquement il y a beaucoup plus de chances pour qu’un système éloigné de l’état d’équilibre, c’est-à-dire de l’état final attendu, tende à le retrouver, plutôt qu’il s’en éloigne.
Bien malgré lui, Boltzmann découvrit également que l’irréversibilité était prouvée dans les transferts de chaleur. Lorsqu’il mettait deux substances de température différentes en contact, la chaleur de la première se transmettait à la plus froide, mais jamais l’inverse.
6. Qu’est-ce que le mouvement brownien ?, 26 mars 2010, 12:56, par Robert Paris
" on avait tendance à croire que l’évolution vers l’équilibre était synonyme de perte d’information, d’une uniformisation du système. Or dés que l’on s’éloigne un tant soi peu de l’équilibre, on assiste à la coexistence de phénomènes d’ordre et de désordre."
Ilya Prigogine
1. Qu’est-ce que le mouvement brownien ?, 27 mars 2010, 09:54, par moshe
" on avait tendance à croire que l’évolution vers l’équilibre était synonyme de perte d’information, d’une uniformisation du système. Or dés que l’on s’éloigne un tant soi peu de l’équilibre, on assiste à la coexistence de phénomènes d’ordre et de désordre."
Ilya Prigogine
7. Qu’est-ce que le mouvement brownien ?, 17 décembre 2016, 08:50, par alain
Comment se fait-il que le mouvement brownien ne soit pas en contradiction avec le principe de la conservation de l’énergie ?
8. Qu’est-ce que le mouvement brownien ?, 17 décembre 2016, 08:50, par R.P.
La quantité d’énergie mise en œuvre par le mouvement brownien est négligeable à l’échelle macroscopique. On ne peut pas en tirer de l’énergie pour réaliser un mouvement perpétuel de seconde espèce, et violer ainsi le deuxième principe de la thermodynamique.
Toutefois, il a été démontré que certains processus biologiques à l’échelle cellulaire peuvent orienter le mouvement brownien afin d’en soutirer de l’énergie. Cette transformation ne contrevient pas au deuxième principe de la thermodynamique tant et aussi longtemps qu’un échange de rayonnement peut maintenir la température du milieu donc la vitesse moyenne des particules. Il faut aussi considérer que la dissipation de ce mouvement brownien sous forme d’énergie utilisable engendre une croissance de l’entropie globale du système (ou de l’univers).
Jean Perrin écrit dans « Mouvement brownien et molécules » :
« Voici donc une agitation qui se poursuit indéfiniment sans cause extérieure.
Il est clair que cette agitation n’est pas en contradiction avec le principe de la conservation de l’énergie. Il suffit que tout accroissement de vitesse d’un grain s’accompagne d’un refroidissement du fluide en son voisinage immédiat, et de même que toute diminution de vitesse s’accompagne d’un échauffement local, nous apercevons simplement que l’équilibre thermique n’est, ici aussi, qu’un équilibre statistique. Mais on doit observer, et cette idée très importante est encore due à Gouy, que le mouvement brownien n’est pas conciliable avec les énoncés tranchants que l’on donne trop souvent au principe de Carnot. »
9. Qu’est-ce que le mouvement brownien ?, 18 décembre 2016, 10:09, par alain
Est-ce qu’Einstein a développé ses idées sur la théorie moléculaire de la chaleur à cause du mouvement brownien ?
10. Qu’est-ce que le mouvement brownien ?, 18 décembre 2016, 10:10, par Robert Paris
En fait non, car il a développé ces idées sans savoir clairement ce qu’étaient les observations du mouvement brownien et il s’est trouvé ensuite seulement que cela correspondait exactement à l’idée de molécules sans cesse en agitation thermique.
L’article d’Einstein de 1905 s’intitule : « Sur le mouvement de petites particules en suspension dans des liquides au repos requis par la théorie cinétique moléculaire de la chaleur » :
« Dans cet article on va montrer que d’après la théorie cinétique moléculaire de la chaleur, des corps de taille visible au microscope et en suspension dans des liquides doivent exécuter des mouvements d’une magnitude telle que ceux-ci peuvent être aisément observés au microscope. Il est possible que les
mouvements discutés ici soient identiques à ce que l’on appelle le mouvement brownien moléculaire ; les données qui me sont accessibles sur ce dernier sont si imprécises que je n’ai pu me former de jugement précis sur la question. »
11. Qu’est-ce que le mouvement brownien ?, 5 mars 2018, 21:54, par Yohanan
Quid de certaines radiations sur le mouvement ?
1. Qu’est-ce que le mouvement brownien ?, 6 mars 2018, 08:34, par Robert Paris
Il y a bien sûr des relations entre mouvement brownien et radiations, si c’est cela que tu voulais dire.
Lire ici
Lire aussi
Lire encore
Lire toujours